摘 要: 分步法电解水制氢是近年来发展出的一种新型电解水技术,通过在电池中增加电子耦合质子缓冲媒介(ECPBs),使得电解水的析氢反应(HER)与析氧反应(OER)不再关联,可以实现H2和O2在不同的时间、不同的地点生成。分步法电解水制氢可以解决传统电解水制氢技术面临的H2和O2互相渗透所带来的安全问题,并为氢气的储运提供新的解决方案。本文综述了近年来在分步法电解水方面取得的进展,详细介绍了分步法电解水制氢电解槽结构原理,分步法电解水制氢中可以选择的ECPBs的种类及特点。根据ECPBs的状态及适用的电解液介质,分别列出溶液态和固态电极形态的ECPBs在酸性电解液以及碱性/中性电解液中对应技术参数。通过进一步对比现有ECPBs的优势及不足,总结了分步法电解水所面临的挑战和潜在的发展方向。
关键词: 分步法电解水制氢;解耦水裂解;电子耦合质子缓冲媒介;氧化还原媒介
氢气作为化工原料广泛应用于化工、能源和材料行业。近几十年来在国内外能源结构的调整的背景下,“氢经济”的概念逐步完善,氢能产业链也逐步清晰。目前市场中氢气主要来自化石燃料蒸汽重整和副产氢,前者排放出大量的二氧化碳,对环境造成了严重的影响。后者受储运限制,仅能在副产氢的企业周边供应氢气。而电解水制氢则有无碳环保和灵活的特点,逐渐受到关注。
随着可再生能源发电比例逐步提高,利用可再生能源制氢将电能转化为化学能,不但可以满足可再生能源的储存需求,还可以提高智能电网的灵活性,为氢燃料汽车加气站提供高纯度氢气,是一种具有前景的能量存储与转化的方式,并得到了示范验证。德国的Energiepark Mainz Power-to-Gas Project(PTG)示范项目,位于Mainz,采用6 MW的基于聚合物质子交换膜电解水(PEMWEs)技术的制氢工厂,与8 MW的风场连接,用于探索PEMWEs的规模化应用及经济性运行模式。
传统电解水制氢主要包括碱性电解水(AWEs)、聚合物质子交换膜电解水(PEMWEs)和高温氧化物电解水(SOEC)。AWEs是已经商业化的电解水制氢技术。但是AWEs不能在高压下运行,负载范围窄、灵活性差,也无法支持大电流运行(一般约400 mA/cm2)。PEMWEs电解槽内部呈强酸性环境,对催化剂及组件的耐腐蚀性要求高,因此投资成本相比较高,限制了其广泛应用。最重要的是隔膜在运行过程中受高压的影响,以及氢气和氧气的互相渗透在隔膜内生成过氧化物或者活性氧,会腐蚀隔膜并降低隔膜寿命。隔膜的损坏进一步导致氢气和氧气渗透的恶化,不但降低电流效率,还带来极大的安全隐患。SOEC制氢技术,效率高、生产速度快,但是需要在高温下运行,对关键材料要求高,因此成本最高,还处于研究阶段。
2013年,Cronin的团队首次报道了分步法电解水。提出了“电子-耦合-质子缓冲(ECPBs)媒介”这一概念。通过缓冲媒介可以将电解水的析氢反应(HER)和析氧反应(OER)分离。近年来分步法制氢的科学概念逐渐成熟,研究人员的结果表明,分步法制氢将水裂解的HER和OER在时间和空间上进行分离,使得制氢和制氧成为两个独立的步骤。首先,分步法电解水制氢可以解决传统电解水H2和O2同步生成,并通过隔膜互相渗透所带来的安全问题。其次,如果使用固态电极作为ECPBs,阴极和阳极之间无需隔膜,还可以被转移运输至加氢站后再完成制氢,也为氢气的储运带来新的替代方案。此外,OER是电解水的速控步骤,传统电解水技术在低负荷下运行时,氧气生成速度过低,甚至低于氧气渗透过隔膜至阳极侧的速度,因此很难直接采用具有不连续性和间歇性的风能/太阳能发电作为制氢的能源。而这种分步法电解水制氢策略使得电解水制氢技术有望直接应用于新能源发电领域,为“弃风弃光”问题提供新的解决方案。
1 分步法电解水原理
分步法电解水是在电解水体系中增加电子-质子缓冲介质(ECPBs),将水的裂解分为两个步骤,第一步接通阳极和ECPBs,OER发生时,阳极产生氧气,释放的电子由ECPBs存储,而ECPBs自身被还原。第二步,将还原态的ECPBs与阴极接通,HER发生时,阴极产生氢气,ECPBs释放电子自身被氧化,见方程(1)、(2)。

结合近年来分步法电解水制氢的研究工作,图1给出了分步法电解水制氢原理结构。通常情况下,由于所使用的ECPBs的状态不同,电池结构可以分为有隔膜和无隔膜两种。当ECPBs为溶液状态时,需要隔膜将电池分隔为两个腔室,其中阳极和阴极电极位于工作室内,而ECPBs则位于工作室对面的辅助室内,如图1(a)所示。如果使用固态ECPBs电极,则电池无需使用隔膜,阳极、阴极以及辅助电极位于同一电池室内,如图1(b)所示。在分别启动第1步和第2步电化学反应步骤时,需要在阳极和阴极之间切换开关并联通电路。
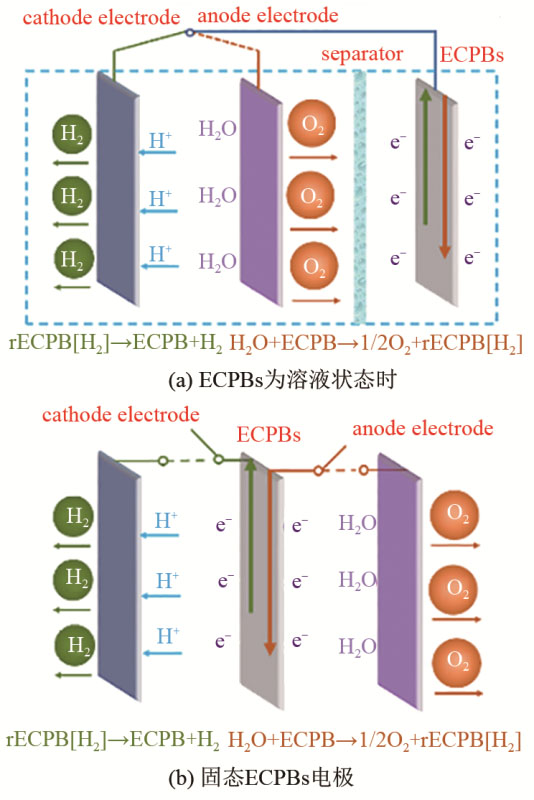
图1 分步法电解水制氢的结构
2 溶液态ECPBs
2.1 酸性介质
在酸性介质下,常使用杂多酸作为ECPBs。例如分子结构式为HnXW12O40(X= P5+、Si4+、 Zn2+)的杂多酸溶液都可作为ECPBs。图2(a)给出了{PW12O40}、{SiW12O40}、{ZnW12O40}的循环伏安曲线,从图中可见,其氧化还原电位电位均位于HER和OER之间,适合作为ECPBs。图2(b)给出了这些杂多酸的转移电子数随溶液pH值变化的情况。
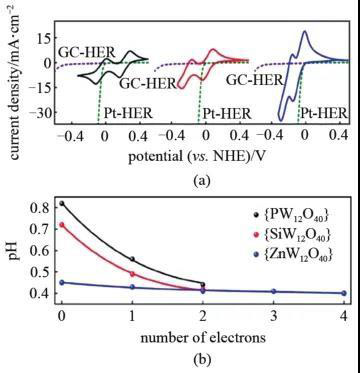
图2 (a) 100 mmol HnXW12O40 (X= P5+,Si4+ 和Zn2+) 扫速50 mV/s的CV曲线;(b) 在不同pH值缓冲溶液中电荷转移数
(H3O+)[H2PMo12O40]的循环伏安曲线如图3(a)所示,由于ECPBs的氧化还原作用,水的析氧反应和(H3O+)[H2PMo12O40]的还原反应与质子化作用相结合,形成(H3O+)[H4PMo12O40]。而进一步的,ECPBs缓冲媒介(H3O+)[H4PMo12O40]的氧化反应则与阴极的析氢反应结合,最终释放出氢气。这里磷钼酸作为ECPBs的还原电压较HER更高,使得阳极的OER可以在更低的电压差下发生,如图OER电压降低了近0.9 V[图3(a)]。同理阴极的HER也有相似情况,如图3(b)所示。
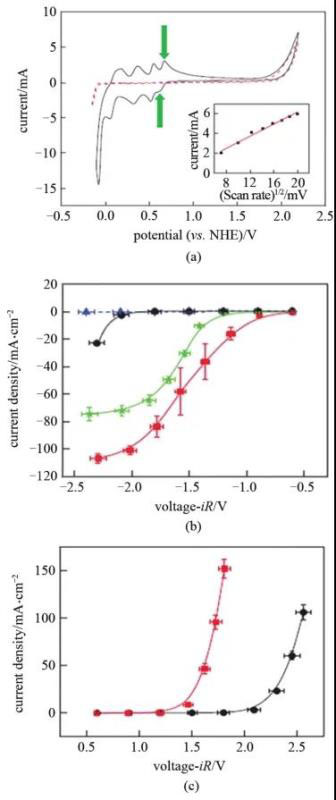
图3 (a) 循环伏安曲线:1.0 mol/L H3PO4+0.5 mol/L磷钼酸(黑色),1.0 mol/L H3PO4(红色);(b) 在两电极体系中HER在铂电极(有ECPB红色,无ECPB黑色)和铂碳电极(有ECPB绿色,无ECPB蓝色)上的极化曲线;(c) 在两电极体系中OER在铂电极上的极化曲线:有ECPB(红色),无ECPB(黑色)
这些杂多酸通常具有很高的分子量,磷钼酸分子量高达1843,硅钨酸分子量为2880,因此质量能量密度低。此外,杂多酸所使用的钼、钨等元素的成本也较高,因此,在ECPBs的设计和选择上,除了考虑其氧化还原电位的适宜性,还应该向低分子量、元素储量丰富廉价的方向发展。对于阴极的HER,在规模化应用时可以选择耐酸腐蚀的过渡金属化合物代替Pt,例如Ni5P4、Ni2P、Mo2C、MoS2、CoP等。
近年来,很多有机物作为电化学储能的活性材料被研究。Cronin的团队分别采用对苯二酚磺酸钾、二酚衍生物蒽醌-2,7-二磺酸(AQDS)来作为分步法电解水的ECPBs,解耦后的HER和OER各自所需的电压差明显降低。不足的是对苯二酚磺酸钾自身稳定性较差(1%衰减率),还会透过Nafion隔膜导致总法拉第效率降低。但是AQDS具有良好的稳定性,每周容量衰减率仅0.06%。
使用ECPBs进行解耦水分解时,由于H2和O2并不是同时产生的,因此气体的纯度很高。但是这也意味着与传统电解水相比,产生H2和O2所需要的时间将翻倍。为了满足分步电解水并减少总时间消耗,Amstutz等报道了一种包含氧化还原流动电池模块的新型分步法电解水设计。与常规的使用单个ECPBs不同,这里的ECPBs是由两种氧化还原介质V(Ⅲ)/(Ⅱ)和Ce(Ⅳ)/(Ⅲ)构成的液流电池模块构成,系统的结构如图4所示,其中模块Ⅰ是传统氧化还原流动电池。在中间位置的氧化还原液流电池在充电过程中,正极侧Ce(Ⅲ)在1.0 mol/L H2SO4介质中被氧化为Ce(Ⅳ),负极侧V(Ⅲ)还原为V(Ⅱ)。在催化剂存在的情况下,Ce和V能够生成氧气和氢气。然后将这些正极电解液和负极电解液分别泵入各自的催化床,在RuO2上生成O2,在Mo2C上生成H2。反应方程如式(3)、式(4)所示。
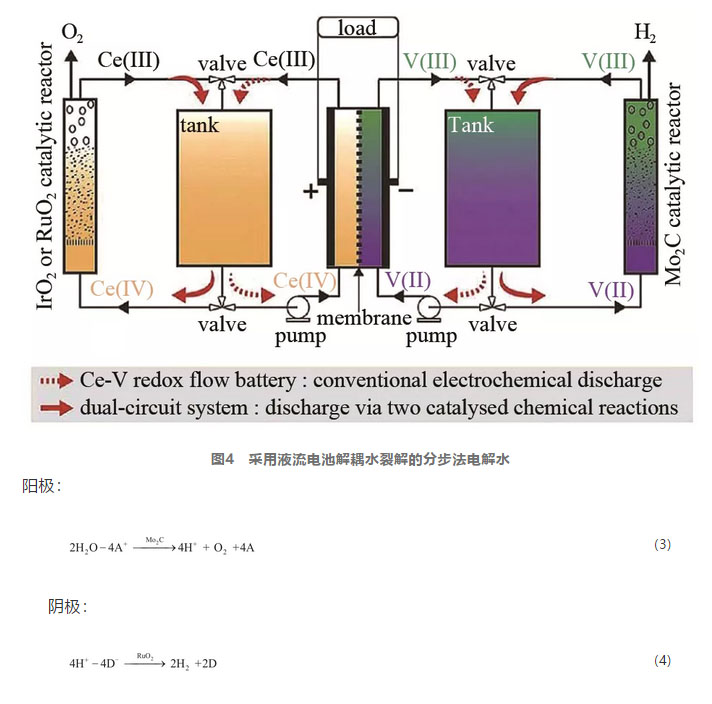
这种将电解水制氢与液流电池结合的系统设计,从液流电池角度来看,可以突破传统液流电池受限于电解液浓度而能量密度低的限制,通过辅助的制氢系统,让电能转化为化学能的同时,化学能再转化为可以独立储运的氢气。由于氢气可以通过储运的方式脱离系统,因此从理论上说,整个系统的容量没有上限。而液流电池充当ECPBs后,使得电解水的OER和HER成为两个独立过程,但是与常规使用一种ECPBs分步法制氢相比,仅解耦了它们在空间上的关联,即HER和OER可以分别在两个独立的电池室内完成,却仍然可以同时发生,这有效缩短了分步法制氢所消耗的时间,使得分步法制氢概念进一步得到优化。
2.2 碱性介质
由于大多数的催化剂在低pH条件下无法稳定存在,这使得可选择的电催化剂非常有限,因此,进一步探索适用于碱性介质下的分步法电解水技术是降低成本和提高性能的有效途径。基于上述考虑,Sun的团队开展了碱性介质下以Na4[Fe(CN)6]作为EPCBs来实现分步法电解水的研究工作。
Na4[Fe(CN)6]在碱性电解液(1.0 mol/L KOH)中具有良好的溶解性,反应速度快。由于阳极OER的产物利用价值低,还可以在工作电极室内加入羟甲基糠醛(缩写为HMF,其氧化态为2,5-呋喃二羧酸,缩写为FDCA)。Na4[Fe(CN)6]的Fe(Ⅲ)/(Ⅱ)氧化还原电位位于HER和OER的电位之间,其电位也低于相应工作电极上HMF氧化的起始电位。则当辅助室内发生Fe(Ⅲ)/(Ⅱ)氧化还原反应,而工作室内则发生HER和HMF/FDCA氧化还原反应。两个室由阴离子交换膜(SELEMION TM,AMV 120 μm)分开。从投资资本的角度来说,使用廉价的催化剂具有规模化应用的潜力。
2.3 中性介质
使用强酸性或强碱性电解质,会对电解槽组件产生腐蚀,因此需要使用耐腐蚀性更好的关键材料,这无形中增加了成本。Sun的团队进一步探索了中性电解液中的分步法电解水的可行性。二茂铁具有很多衍生物,其中(二茂铁甲基)三甲基氯化铵(FcNCl)的氧化还原反应不依赖于质子,适用于中性电解液中作为分步法电解水的ECPBs。
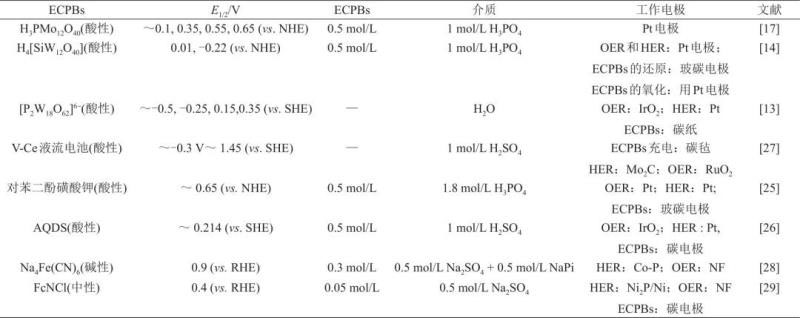
表1中给出了几种典型的溶液态ECPBs,以及它们在分步法制氢实验中的关键的技术参数。
表1 溶液态ECPBs关键技术参数及测试条件
3 固态电极作为ECPBs
分步法裂解水所用的ECPBs为溶液态时,需要隔膜将电池分成两个独立的腔室。这不仅增加了隔膜这部分成本,也由于隔膜的存在增大电池内阻。王永刚团队研究了多种使用固态电极作为ECPBs的分步法电解水体系。
3.1 酸性介质
一些具有电化学活性的有机物,例如聚三苯胺(PTPAn)、pyrene-4,5,9,10-tetraone(PTO)等,可以作为酸性介质下的ECPBs,来实现酸性介质下的分步法电解水制氢。PTPAn可制成固态电极来作为ECPBs,使HER与OER成为两个独立过程。在0.5 mol/L H2SO4溶液中,PTPAn有两种构象异构体,对应于两对氧化还原峰,分别位于0.5 V/0.48 V和0.6 V/0.58 V(vs.Ag/AgCl)[图5(a)]。PTPAn固态电极作为ECPBs具有许多优点,尤其是PTPAn通过电化学吸附/解吸阴离子并结合电子转移来储存电荷,与电解液的质子浓度无关,不会改变电解液pH,且存储容量远高于杂多酸。计时电位测量结果进一步证明了PTPAn在分步法电解水中具有良好稳定性。
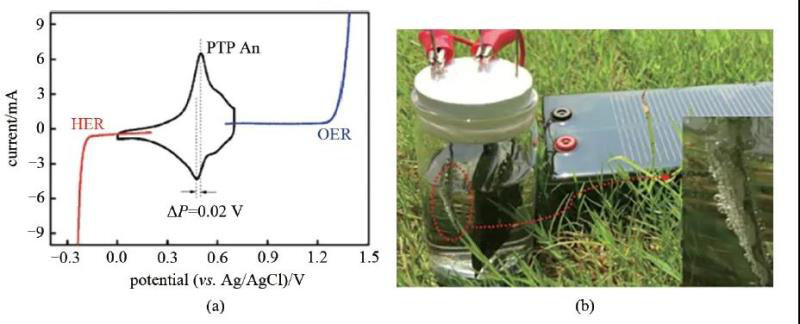
图5 (a) PTPAn的CV曲线,HER的LSV曲线(红线)及OER的LSV曲线(蓝线);(b) 演示实验照片
3.2 碱性介质
王永刚团队首次报道了碱性介质下使用固态氢氧化镍电极的分步法电解水。图6显示了氢氧化镍电极在碱性溶液中的氧化还原峰,位于氢氧化镍电极在碱性溶液中的HER曲线和镀铂钛电极在碱性溶液中的OER曲线之间,这符合ECPBs的特点。在外部电压作用下,第1步发生[Ni(OH)2/NiOOH]-HER过程。通常情况下氧气的收集价值不高,因此可以通过在第2步中用NiOOH/Zn电池的放电过程,或者NiOOH-液态燃料电池的放电过程来取代[NiOOH/Ni(OH)2]-OER过程,这种设计方案可以将NiOOH存储的化学能进一步转化为电能进行使用,而不是获取无用的氧气。在第1步中仍然是生成H2和Ni(OH)2氧化至NiOOH。NiOOH/Zn电池后续放电过程是将NiOOH还原为Ni(OH)2和锌阳极氧化的过程。NiOOH/Zn电池的理论能量密度约280 W·h/kg。

图6 氢氧化镍电极在扫速为5 mV/s时的析氢(HER)循环伏安曲线(a)和商业化电极(铂包覆钛网;二氧化钌包覆钛网)在扫速为5 mV/s时析氧(OER)线性扫描伏安曲线(b)
此外,Tsutsumi等报道了一种采用三种固体电极Ni(OH)2/MnO2/LaNi5组合的演示电池,MnO2作为分步法电解水制氢的ECPBs,可以通过两步电化学循环分别产生H2和O2。
相比于溶液态的ECPBs,使用固态电极的分步法电解水无需使用隔膜。在PEM制氢中,膜电极(MEA)在成本中占比约24%,因此可以达到节约成本的目的。同时,还可以降低由隔膜带来的电阻,提高电池性能。而且固态NiOOH电极适用于碱性电解液中,可以使用廉价催化剂替代贵金属催化剂,这有望进一步降低电池成本。
Grader等也开展了类似的研究工作。他们探索了以光能驱动分步法电解水的第1步反应,光电阳极(赤铁矿,α-Fe2O3)-Ni(OH)2发生OER反应,NiOOH被还原至Ni(OH)2。第2步中由光伏发电驱动反应,Ni(OH)2氧化为NiOOH,同时阴极发生HER反应。由于一般情况下无需收集氧气,阳极室为透明材质且无需密封。ECPBs阴极室采用表面镀铂的钛网做工作电极,Ni(OH)2电极做辅助电极。由于阴极室仅制备氢气,因此电极之间无需隔膜,但是需要密封设计,电池结构如图7(b)所示。如果进行产业化应用,可以选择镍基催化剂取代铂。
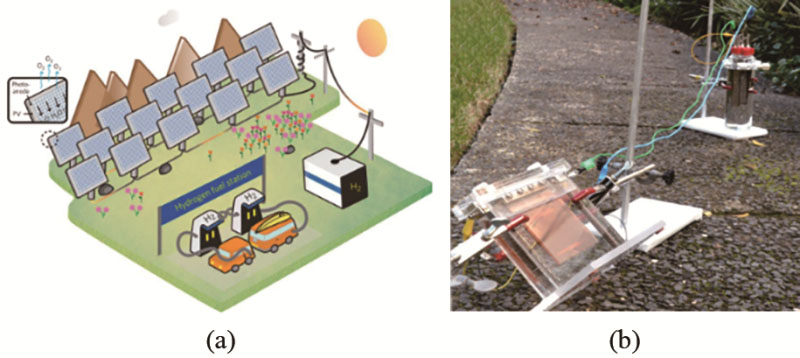
图7 (a) PEC-PV-分步法集中制氢加氢站的概念图;(b) 户外分步法PEC-PV单电池串联结构演示电池
Grader等进一步研究并提出了集中制氢的概念,通过将ECPBs的容量设计成理论容量的2倍或者更多倍,以减少在阳极和阴极之间切换的频率,提高运行效率。并且对辅助电极在阳极和阴极之间的切换周期进行了优化设计,这一概念通过实验室规模的电解装置进行了验证和演示。装置采用了镍阳极和阴极,由一个迷你PV模块供电,独立光解制氢(solar to hydrogen,STH)效率为7.5%。
这种光伏供电的分步法-集中式制氢设计,使用氢氧化镍电极做为ECPBs,电池无需使用隔膜,可节约成本,降低内阻。整个系统可以设计成多模块,通过模块的转移实现氢气的运输,也不需要建设氢气输送管路。
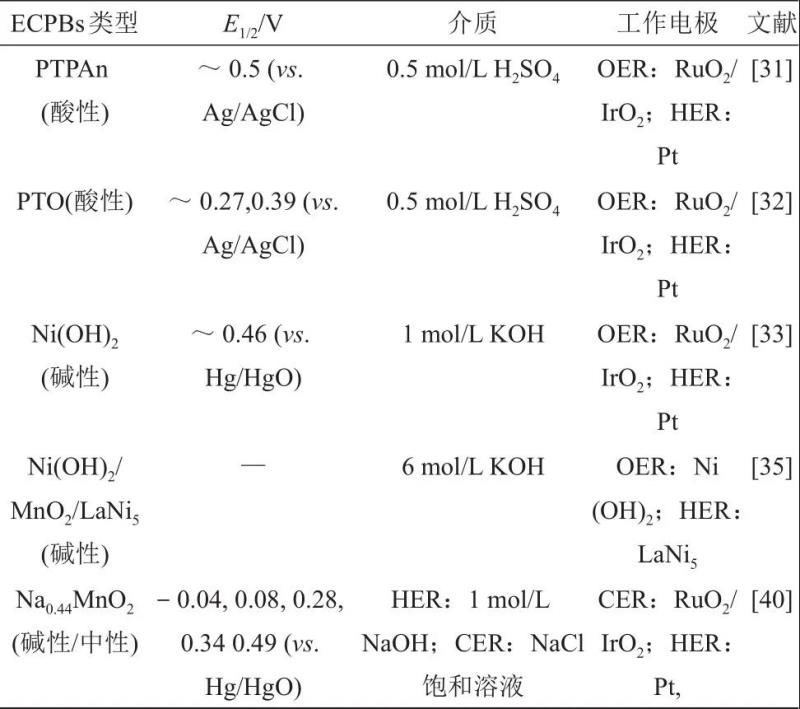
表2中给出了几种典型的溶液态ECPBs,以及它们在分步法制氢实验中的关键的技术参数。
表2 固态电极ECPBs关键技术参数及测试条件
4 分步法电解的其他应用
王永刚团队还将分步法电解的概念应用到其他电解工艺中。传统氯碱工业中,阳极生成氯气,阴极生成氢氧化钠和氢气。两极之间通过石棉隔膜分隔开,阻止氯气与氢氧化钠发生反应降低反应效率。通过在电解过程中加入锰酸钠电极作为ECPBs,将同时发生的氯气生成和氢气生成反应,解耦成为独立发生的两个反应,因此电池两极间无需再使用隔膜。
对锰酸钠电极进行线性伏安扫描测试,如图8所示,其氧化还原峰正好位于HER和CER的中间区域。锰酸钠在水系溶液中具有良好的钠离子嵌入脱出能力,因此非常适合作为ECPBs。
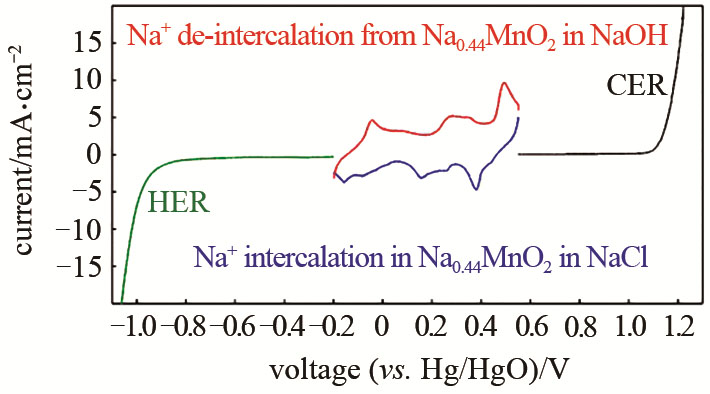
图8 锰酸钠电极在1 mol/L NaOH溶液(红色)和饱和NaCl溶液(蓝色)中的LSV曲线,扫速为2 mV/s。铂包覆钛网电极在1 mol/L NaOH溶液中的析氢(HER)LSC曲线(绿线),二氧化钌包覆钛网在饱和NaCl溶液中的析氯(CER)LSV曲线(黑线),扫速为2 mV/s
5 展 望
分步法电解水制氢,由于氢气和氧气独立制备,因此能够适应风力发电或者光伏发电场的功率变化,是具有前景的能量存储与转化方式。分步法电解水在应用中,可以在可再生能源发电场内完成H2O + ECPB 图片 1/2O2 +rECPB[H2]这步骤反应,然后再将电池运输至需要补充氢气的加氢站,在加氢站完成rECPB[H2] 图片ECPB+H2这一步骤。这种设计在制备氢气的同时,还兼具储存氢气的功能,如果电池设计成移动柜模式,则以可再生能源发电场为中心,向四周辐射建设加氢站,按需求输送氢气。与传统电解水制氢设备相比,可以减少制氢设备投入的总量,提高设备的利用率。与传统氢气储运方式相比,固态电池的运输安全性能更高。
但是,分步法制氢还是一个崭新的概念,它仅在实验室实现了演示。表3中给出了现有的ECPBs在应用中的技术特点,通过对比可以看出,分步法电解水制氢仍然需要加强基础研究,深入研究电极之间动力学匹配性、电化学反应过程中涉及的机理。在工艺开发设计方面需要开展电池模组结构设计、电池运行控制策略等方面的研究。此外,最近的几项研究也表明,这种解耦的电解策略不仅限于水分解,还可以应用于其他电解工艺领域。尽管溶液态和固态的氧化还原媒介在很宽的pH范围中都有报道,但是,电子-质子缓存媒介数量仍然较少,可应用的电化学窗口也较狭窄。随着人们对利用氧化还原介质进行各种电化学反应的兴趣日益增加,更多的氧化还原媒介有望被探索研究,早日实现分步法电解水在工程化领域的应用。
表3 不同类型ECPBs在应用中的技术特点

引用本文: 苏秀丽,廖文俊,李严.分步法电解水制氢的机遇与挑战[J].储能科学与技术,2021,10(01):87-95.
SU Xiuli,LIAO Wenjun,LI Yan.Opportunities and challenges of hydrogen production with decoupled water electrolysis[J].Energy Storage Science and Technology,2021,10(01):87-95.
通讯作者:苏秀丽(1978—),女,工程师,主要从事电化学器件、储能技术、全钒液流电池等方向研究,E-mail:suxl@shanghai-electric.com。





