中国储能网讯:
摘 要 全钒液流电池具有寿命长、安全性高、能量控制管理简单、功率和容量完全解耦等优点,适用于新型电力系统中新能源发电波动平滑、削峰填谷、稳压调频等应用场景,近年来已经开始规模化推广应用。由于隔膜等关键材料特性、电堆及管道系统结构、电解液成分等全钒液流电池的固有特点,其运行过程中存在容量衰减问题,为保障全钒液流电池寿命,提高能量效率,减少正负极离子浓度及价态再平衡等运维频次,国内外对全钒液流电池容量衰减抑制进行了大量研究。本文从容量衰减机理和抑制方法角度分析了全钒液流电池容量衰减影响因素,总结了不同应用工况下水和钒离子的迁移、自放电和析气副反应、温度与浓度等对容量衰减影响的研究现状,阐明了容量衰减机理。重点分析了隔膜、电解液相关材料应用工况对容量衰减抑制的影响规律,以及基于流量、充放电制度、活性物质浓度调整等参数的容量衰减抑制技术,展望了基于应用工况的全钒液流电池容量衰减抑制新兴技术,为全钒液流电池运行中的电解液容量保持提供指导依据。
关键词 全钒液流电池;容量衰减;抑制技术;工况
全钒液流电池作为面向电网级储能应用而开发的一种化工型电化学储能,由于其具有运行安全、可深度充放电、循环寿命长、功率容量相互解耦等优点,在新能源接入、新型电力系统建设等领域具有广阔的应用前景。全钒液流电池最早由澳大利亚新南威尔士大学的Skyllas-Kazacos教授于1985年提出,主要由电解液、双极板、电极、隔膜等关键材料构成。在运行时,分别以电解液中不同价态的钒离子作为正负极的氧化还原电对,正、负极泵将电解液输送至对应的半电池中,钒离子在电极上进行氧化还原反应,通过钒离子的价态转变实现电能的存储与释放,避免由不同种类离子跨膜渗透而造成的交叉污染,具有使用寿命长、可靠性高等优点。但由于隔膜、电解液这些核心材料的存在,全钒液流电池在长期循环中存在着电解液失衡现象,不可避免地出现容量衰减问题。工程上通常采用混液再平衡的方式恢复容量,即周期性地将负极和正极电解质重新混合,使正负侧的浓度和体积达到平衡,恢复各价态钒离子的不对称转移造成的部分容量损失,延长循环寿命。然而析氢和氧化导致的电解液价态失衡问题仍然存在,为恢复电解液综合价态,需要电解或加入还原剂,对混合后的电解液进行电荷调整,产生了额外的时间、材料等运维成本,并且正负极混液后也存在着零压启动问题。因此全钒液流电池容量衰减抑制技术引起了研究人员的重视,研究人员通过建立各种交叉动力学和反应动力学模型研究容量衰减机理,采用各种抑制容量衰减的策略,如调节流量、改变充放电电流、平衡渗透压、修饰隔膜、优化电解液等抑制容量衰减。本文综述了当前全钒液流电池容量衰减抑制技术的相关研究,结合钒电解液的容量衰减机理,深入探讨了各种衰减抑制方法的可行性和局限性,展望了容量衰减抑制未来研究开发的潜在方向。
1 容量衰减分析
全钒液流电池在运行时,正、负半电池中的钒离子因跨膜渗透而失衡,这种现象的出现对长期循环后电池容量的下降有重要影响。后续,水分子迁移、自放电、析气反应、钒析出等其他因素也会导致电池容量的损失[7-10]。此外,工作条件如工作温度、电解液流量、电流密度、活性物质浓度等因素也会影响电池运行容量的衰减。
1.1 容量衰减机理分析
1.1.1 钒离子的迁移
在全钒液流电池中,电能以化学能的方式存储在不同价态钒离子的硫酸溶液中,正极电解液中以V(Ⅳ)/V(Ⅴ)作为活性物质电对,负极电解液中以V(Ⅱ)/V(Ⅲ)作为活性电对。电池启用时,外接的循环泵分别将正、负极电解液导入电堆,使其在正、负极储液罐和对应半电池的闭合回路中循环,电解液流经电极表面并于此发生氧化还原反应,电子转移形成电流,同时H+在两个半电池之间跨膜迁移以维持电荷平衡,使溶液中的化学能转换成电能。充放电循环时的反应过程完全可逆,反应如下:
正极反应:
VO2+ + H2O - e- ⇌ VO2+ + 2H+ E0 = 1.004 V (1)
负极反应:
V3+ + e- ⇌ V2+ E0 = -0.255 V (2)
总反应:
VO2+ + V3+ + H2O ⇌ VO2+ + V2+ + 2H+ E0 = 1.259 V (3)
其中,隔膜位于电池的中心,将电池分为正负两个半电池,理想下的隔膜应具有高选择性,允许H+通过的同时完全阻碍钒离子的跨膜渗透,但目前全钒液流电池所使用的隔膜无法保证这一点,在长期循环中不可避免地会出现正、负极钒离子的跨膜渗透,钒离子的渗透行为使电池容量随循环逐渐衰减,因此钒离子在膜间的渗透机理是电池容量衰减重要的研究方向。研究表明,在充放电循环中,隔膜两侧不同的浓度梯度是驱动钒离子跨膜渗透的主要原因,并且不同价态钒离子在膜上的扩散速率不同。Sun等人测定了全钒液流电池中钒离子在全氟磺酸膜(Nafion 115)上的扩散系数[图1(a)],其顺序为V2+> VO2+> VO2+> V3+,具体数据见表1。
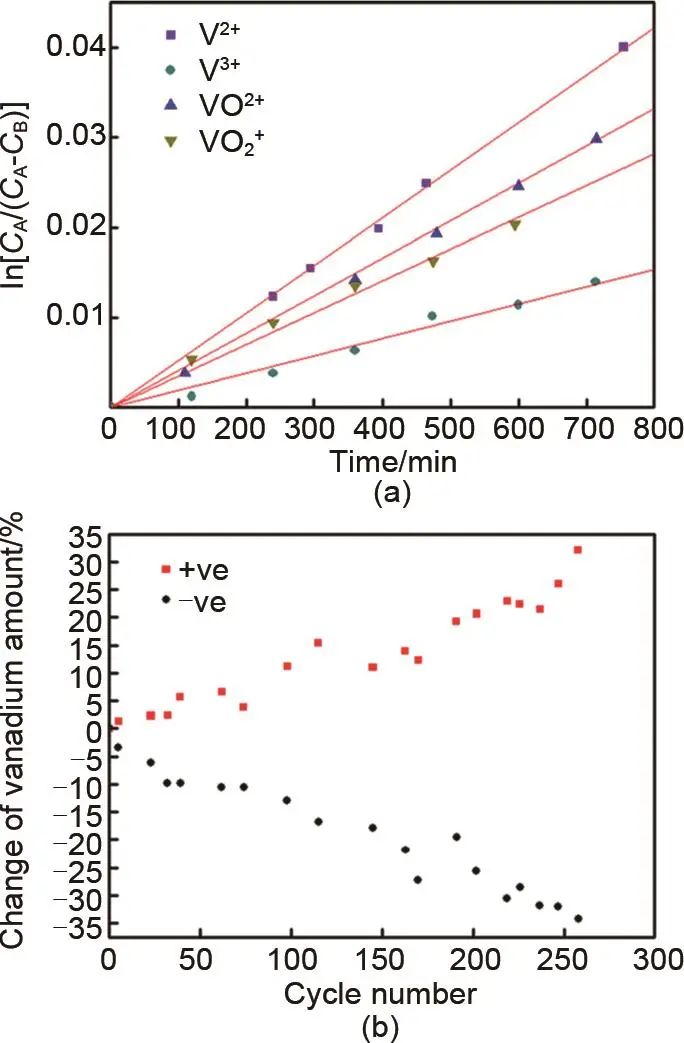
图1 (a) ln [CA/(CA-CB)]与t的关系图;(b) 长期充放电循环中钒离子总量的变化
表1 钒离子扩散系数

如图1(b)所示,在实际的充放电循环中,连续300次循环时,正极中钒离子含量增加,负极钒离子含量下降,在150次循环后正极钒离子总量增加10%,250次时增加25%,这是由于充放电时负极中的V2+和V3+的转移速率大于正极中VO2+和VO2+的转移速率,从而导致了钒离子从负半电池向正半电池的净转移。随着循环的进行,越来越多的钒离子在正极半电池中积累,造成电池活性物质失衡。此时,负极电解液成为“极限电解液”,体积和活性物质数量下降,而正极电解液中越来越多的钒离子无法参与充放电过程,循环过程中电池的钒离子利用率下降,导致了容量的衰减。
1.1.2 水迁移
在电池的充放电循环过程中,电解液中活性物质浓度逐渐失衡,与此同时,两个电解液罐内的溶液体积也会逐渐失衡,并且失衡的程度与循环时间成正比,水通过膜的交叉被认为是造成这种现象的主要原因。长期循环时电解液的体积变化如图2(a)所示,正极电解液体积持续增加而负极电解液持续降低,与钒离子迁移规律相同,在150次循环后正极体积增加10%,250次时增加25%。图2(b)给出了连续8次充放电循环中电解质的体积变化,在单个充放电循环中,正极的体积在充电过程中减小,而负极的体积在放电过程中减小,说明水在充电过程中从正极转移到负极,并在放电过程中从负极转移到正极,但由于其转移量的不同,循环后水的净转移趋势为由负极流向正极,该研究中单次循环时输送到正极的净水量平均为24 mL。引起水转移的所有因素如图2(c)所示,在钒离子和质子跨膜传输时,均会携带结合水进行迁移,其中不同价态钒离子携带的水分子数量不同,此外,水迁移还受到渗透压的驱动作用,在自放电过程中两者对水迁移的贡献比重约为1∶3。
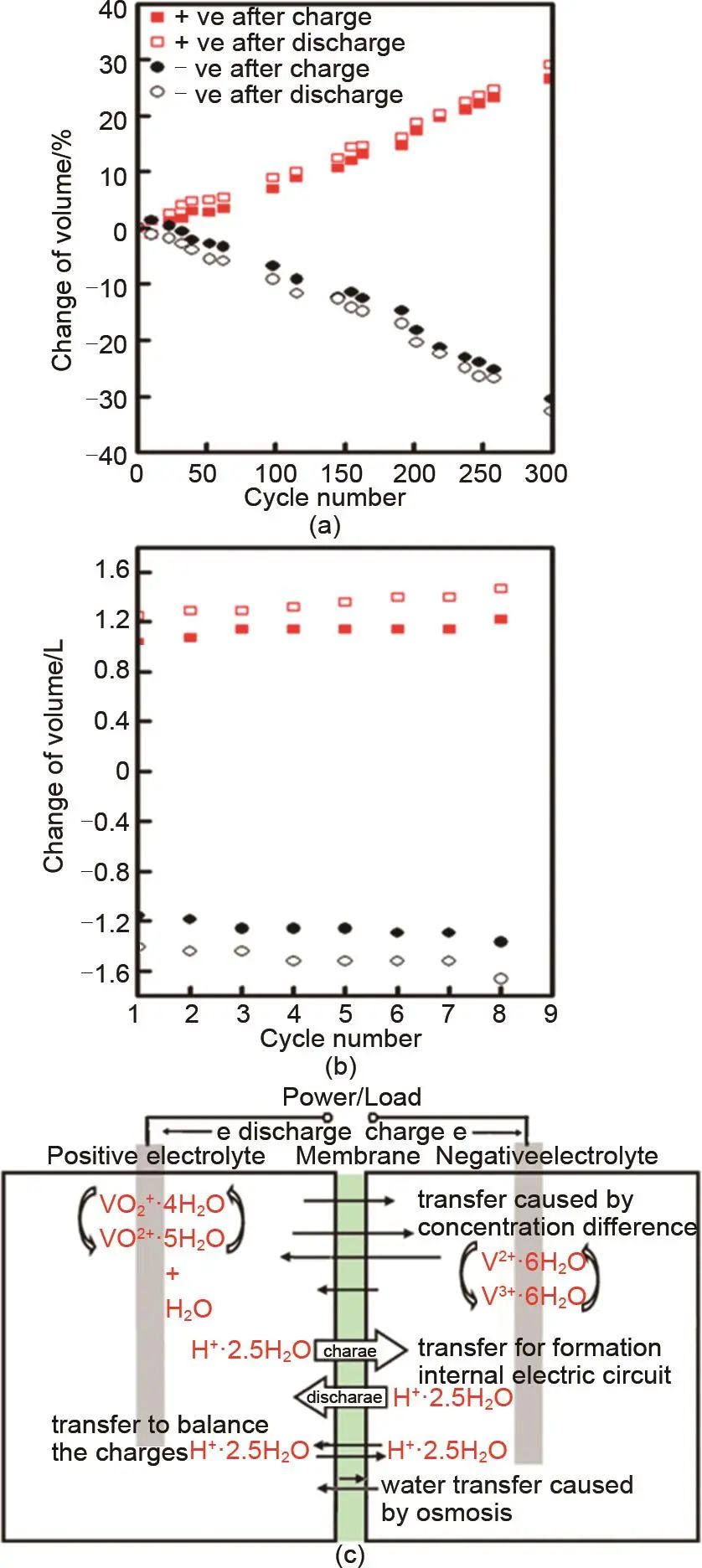
图2 (a) 长期循环时的体积变化;(b) 8次循环中的体积变化;(c) 自放电过程中水和钒离子的转移示意图
水迁移所导致的体积失衡加剧了电解液的浓度失衡,其增加了一个半电池中的电解液浓度,同时稀释了另一个半电池中的电解液,扩大了浓度差,降低了钒离子的利用率,并可能导致钒离子在高浓度半电池中的沉淀。在充放电循环中,由于产生了钒离子和水分子的持续交叉,工程上需要定期重新平衡电解液,以恢复全钒液流电池的容量,从而增加了运维成本。
1.1.3 副反应
钒离子的跨膜渗透现象会造成电解液溶液的浓度失衡,降低钒离子的利用率。由于价态不同,跨膜扩散后的钒离子将与另一个半电池中原有的钒离子进行氧化还原,产生不期望的自放电副反应,导致两个半电池电解液的综合价态失衡,容量产生衰减。钒离子扩散后正负极可能发生的自放电反应如下:
在正极:
V2+ + 2VO2+ + 2H+⇌ 3VO2+ + H2O (4)
V3+ + VO2+ ⇌2VO2+ (5)
在负极:
VO2+ + V2+ + 2H+ ⇌ 2V3+ + H2O (6)
VO2+ + 2V2+ + 4H+ ⇌ 3V3+ + 2 H2O (7)
由上述反应方程可知,虽然V2 +和V3 +在正极的扩散消耗了不同数量的VO2+,但最终在负极积累了相同数量的不可用V2+。同样,VO2+和VO2+在负极的扩散消耗的V2+量不同,但最终在正极积累的不可用VO2+量相同,如图3所示,无论钒离子的扩散速率如何,在一定的电解液净通量下,不可用钒离子的累积量保持不变。
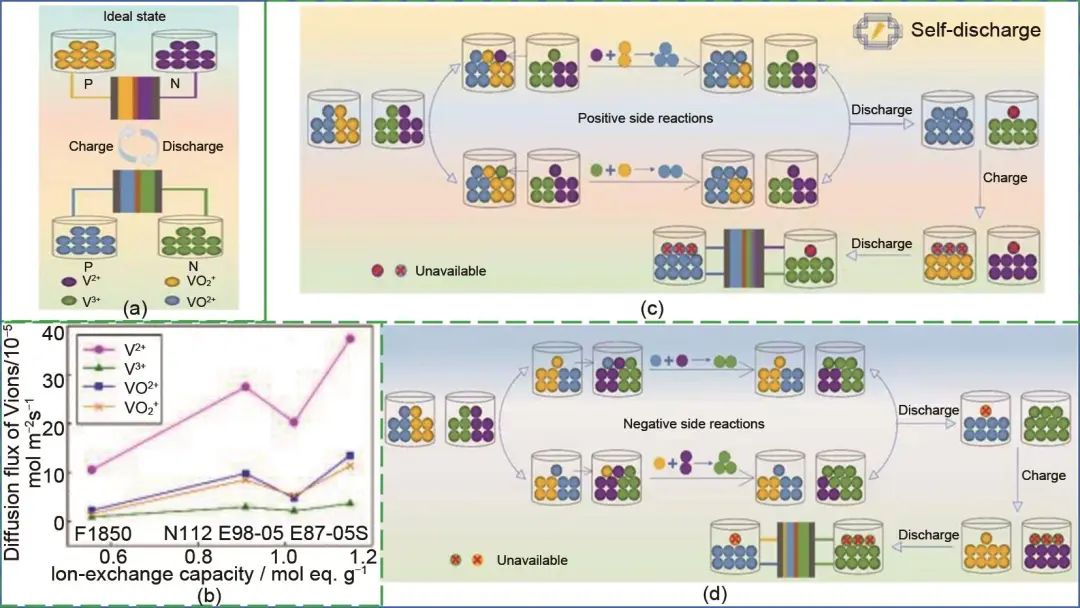
图3 (a) 理想条件下的充放电示意图;(b) 不同钒离子通过膜的扩散通量;(c) V2+/V3+和 (d) VO2+/VO2+在实际循环过程中的自放电反应示意图
正、负半电池中发生的自放电反应导致氢离子的大量损失,削弱了全钒液流电池中的电化学反应。这增加了电压损失,进一步破坏了钒离子正负价态之间的平衡。因此,内部能量损失发生,导致容量衰减。
除了钒离子自放电反应外,电解液中的水在电极上会发生电解反应,产生氢气和氧气,这些副反应也是导致容量衰减的重要因素之一,在负极处,发生如下析氢反应:
2H+ + 2e- ⇌ H2 (8)
析氧反应发生在正半电池中,反应如下:
2H2O ⇌ O2 + 4e- + 4H+ (9)
进一步地,电解液中的溶解氧会对V2+造成化学氧化反应:
2V2+ + O2+ 4H+ ⇌ 2V3++ H2O(10)
处理失衡的最佳方式取决于造成失衡的原因。对于自放电副反应来说,钒离子从电池一侧净转移到另一侧造成浓度不平衡,可以通过混合电解液来纠正。而由钒离子氧化或析气等副反应引起的价态不平衡则只能通过更复杂的化学或电化学方法来恢复。
1.1.4 钒沉淀
高浓度的钒电解液并不稳定,V(Ⅴ)在高温下会有部分结晶析出。葛灵等人通过单因素法分析考察了不同初始V(Ⅴ)浓度、硫酸浓度和磷酸浓度对电解液稳定时长与剩余钒离子浓度的影响,测试结果表明在50 ℃,当初始钒离子在浓度2.0 mol/L以下时,电解液稳定时长与钒电解液为1.6 mol/L时基本一样,当钒离子浓度≥2.2 mol/L时,稳定时长变短,沉淀会更早生成,这是因为存在更多的VO(OH)3分子,造成五氧化二钒沉淀出现。研究还表明,硫酸对剩余钒离子浓度影响不大,但当其浓度超过3.0 mol/L时,电解液稳定时长显著下降,不利于钒电解液的长期使用。
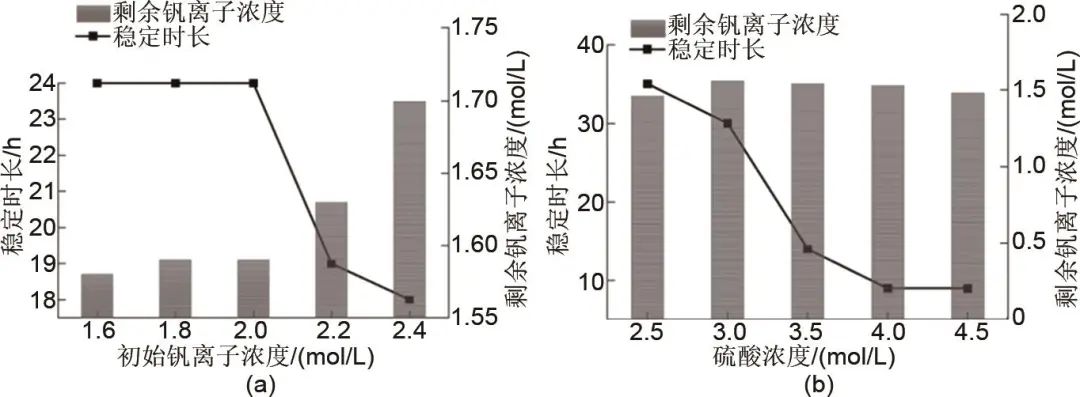
图4 (a) 钒离子浓度对稳定性的影响;(b) 硫酸浓度对稳定性的影响
具体来说,在电池正极中高价态的V(Ⅳ)/V(Ⅴ)以含氧离子VO2+和VO2+的形式存在,VO2+易水解生成V2O5沉淀,该沉淀难溶解恢复,因此维持正极电解液中V(Ⅴ)的稳定性尤为重要。沉淀反应如下:
(2VO2(H2O)3)+⇌VO(OH)3+H3O+ (11)
2VO(OH)3⇌V2O5·3H2O (12)
有研究表明,上述过程为吸热过程,且随着温度升高而加速。Wang等人对钒电解液的广泛温度适应性进行了更详细的研究,他们报道了V2+、V3+、VO2+、VO2+电解液在不同总钒浓度和H2SO4浓度下独立稳定的温度范围,分析得出钒离子的稳定性受由总钒浓度控制的“溶解度效应”与H2SO4浓度控制的“冰点效应”的耦合影响。高浓度的H2SO4有利于V(Ⅴ)的高温稳定性,但不利于V(Ⅱ)的低温稳定性,同时虽然高H2SO4浓度提高了V(Ⅴ)离子的溶解度和热稳定性,但钒离子的流动速度由于黏度的增加而降低,从而导致电极极化较大,降低全钒液流电池系统的能量效率与放电容量,研究认为电解液中钒浓度为1.4~1.6 mol/L,硫酸浓度为2.0~2.5 mol/L是合适的选择。
1.2 影响容量衰减的不同工作条件
1.2.1 工作温度
全钒液流电池中存在着钒离子的氧化还原反应,工作过程中涉及热反应,由此产生的温度变化不仅会影响电解液本身的稳定性,还会对电极上的一系列电化学反应产生影响。随温度升高,电池材料腐蚀、副反应及钒沉淀产生的速度加快,进一步导致了容量的衰减。
值得注意的是,离子的扩散速率依赖于温度,不同温度下各价钒离子的扩散速率不同。Tang等人关联了钒离子扩散与自放电热的相互作用,通过耦合自放电反应的能量平衡和揭示钒离子通过膜交叉的质量平衡,进一步发展了热模型。该模型采用阿仑尼乌斯方程来模拟全氟磺酸膜Nafion 115中钒离子扩散系数对温度的依赖关系,可以预测采用该膜的全钒液流电池中的电解液温度和容量损失。Badrinarayanan等人在上述热模型的基础上建立了一个扩展的动态模型,得到了不同温度下各种膜的扩散系数(图5)。从图中可以看出,随温度上升四种价态的钒离子扩散速率均有提升,而不同类型隔膜中钒离子的扩散系数大小关系发生了改变。随后利用初始模拟的浓度预测电池容量,并通过该容量来确定不同温度下交叉扩散造成的容量损失(图6)。如图所示,电池的容量损失随温度的升高而增加。Karrech考虑影响电池行为的多物理场的耦合过程以及材料特性随温度的变化提出了改进的钒电池模型,并使用该模型来预测动态热化学行为。研究表明,提高温度具有提高扩散和离子迁移率,增强钒离子氧化动力学,降低欧姆电阻和浓度过电位,降低电解质黏度等效果,从而进一步提高电池的性能。然而,高温往往会带来不利影响,包括容量损失,活性物质交叉增加,自放电加剧,以及严重的挥发反应,降低库仑效率和容量保持率。
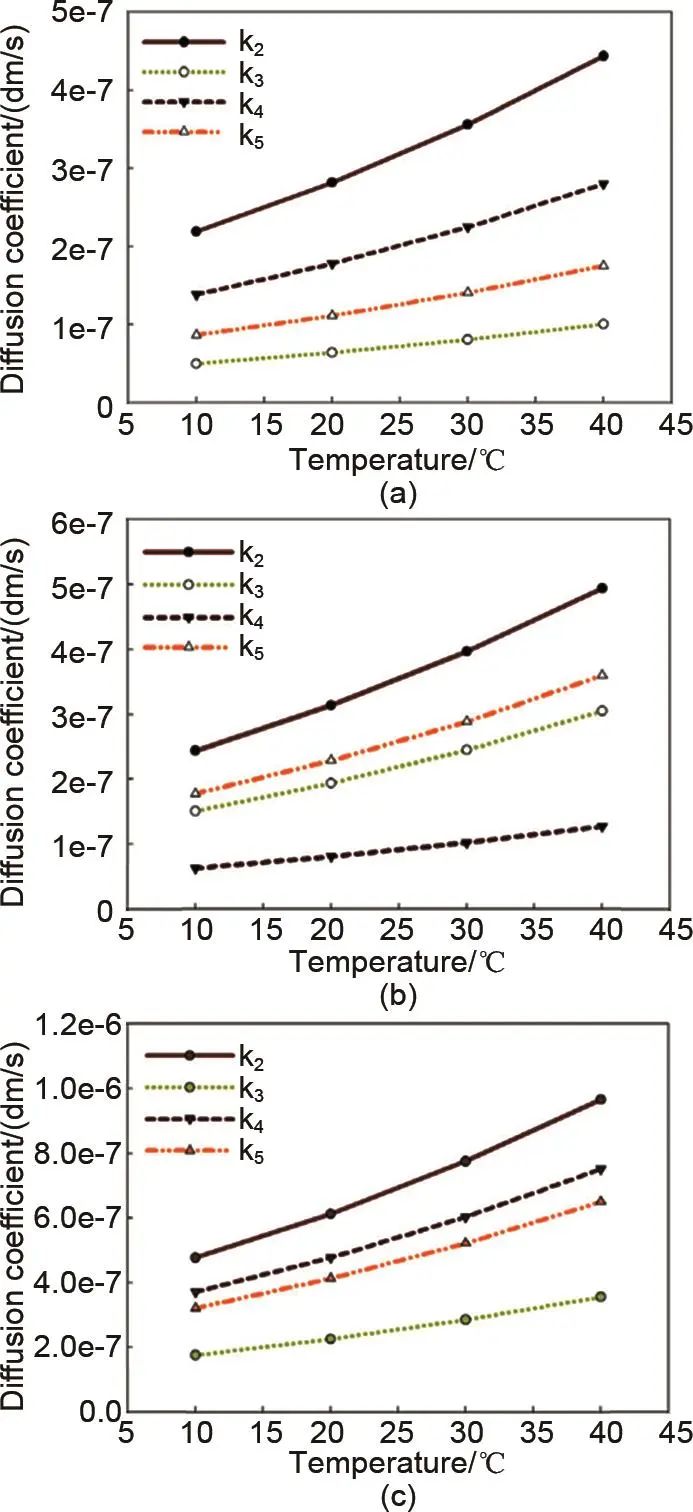
图5 不同温度下各膜的扩散系数(a) Selemion CMV;(b) Selemion AMV;(c) Nafion 115
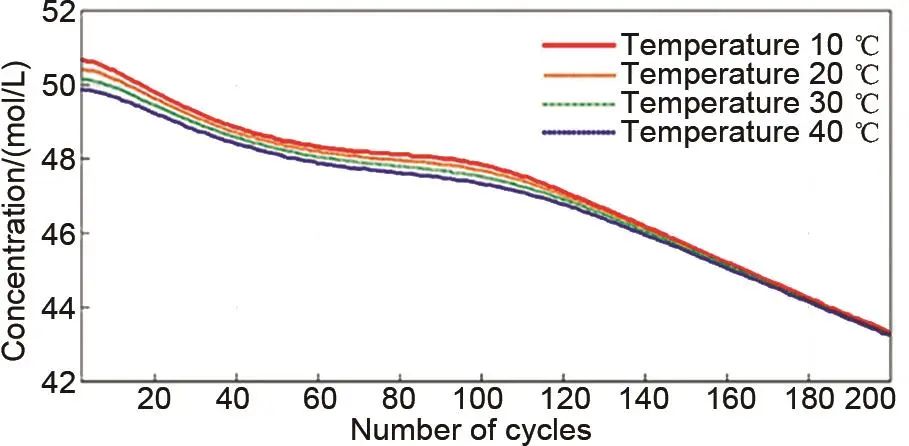
图6 不同温度下Nafion 115膜的容量衰减
热效应在电化学体系中不可避免,全钒液流电池在放电时持续放热升温,由于温度对于电池本身的电化学反应、钒离子扩散以及电解液本身物化性能均造成影响,因此需要对其进行严格控制。对于容量来说,温度的控制需要基于以下两个方面。一方面在保证钒离子不沉淀的情况下提高温度,这有利于钒电池性能的提升;另一方面,基于钒离子的扩散系数,选择钒离子净迁移量最小时的温度,这有利于钒电池容量的保持。
1.2.2 电解液流量
除工作温度外,电解液流量也显著影响电池内部的钒离子浓度分布。王瑄等人对局部供液不足时钒离子的浓度变化进行了考察,所用模型及浓度分布如图7所示。从图中可以看出,缺液时电极中钒离子浓度差异很大,相较于正常工况,此处电位分布也有明显改变。电位的变化不仅影响氧化还原主反应,还可能会加剧副反应的进行。
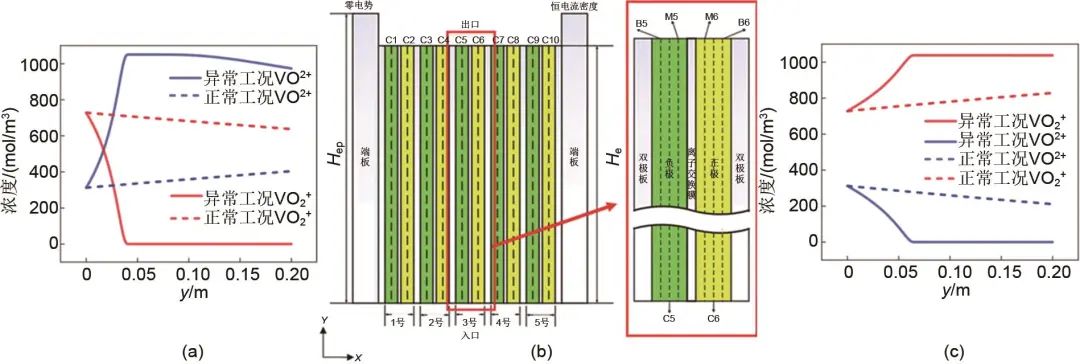
图7 (a) 放电与 (c) 充电工况下正极VO2+/VO2+浓度沿C6分布,(b) 全钒液流电池电堆模型图
在低流量下,电解液的流动速度较慢,电池内部的浓度梯度增大,使得电解液在半电池某些区域积累而无法充分反应,增大浓差极化并且降低电解液中活性物质的利用率,从而降低初始的电解液容量。高流量时,电解液的流动速度较快,正、负极上反应物钒离子浓度与生成物钒离子浓度的差异逐渐减小,反应过程中浓差极化的减少,降低了电压损失,电解液的初始容量得以提升。但流量过大时,钒离子的跨膜扩散通量也会增大,反而加剧全钒液流电池容量的衰减。因此,寻找最佳流量对于保持电池性能和防止容量衰减至关重要。
1.2.3 电流密度
离子在电场作用下跨膜传输的驱动力不仅包括浓度梯度,还包括电位梯度(电场)。浓度梯度驱动的离子扩散通量总是由高离子浓度区向低离子浓度区扩散,其大小与离子浓度梯度成正比。电场驱动下阳离子迁移通量从高电位区向低电位区迁移,而阴离子迁移通量与电位梯度相反。Luo等人采用以钒和铁氧化还原对为电活性物质的液流电池,研究了钒离子在电场作用下的输运行为。如图7所示,电场在充电过程中加速了钒离子从正向负的迁移,减少了钒离子从负向正的迁移,在放电过程中则反过来影响了钒离子的迁移。此外,施加在电池上的高电流密度将导致膜上的高电压降,在较高的温度下,促进或抑制钒离子输运的作用进一步增强。
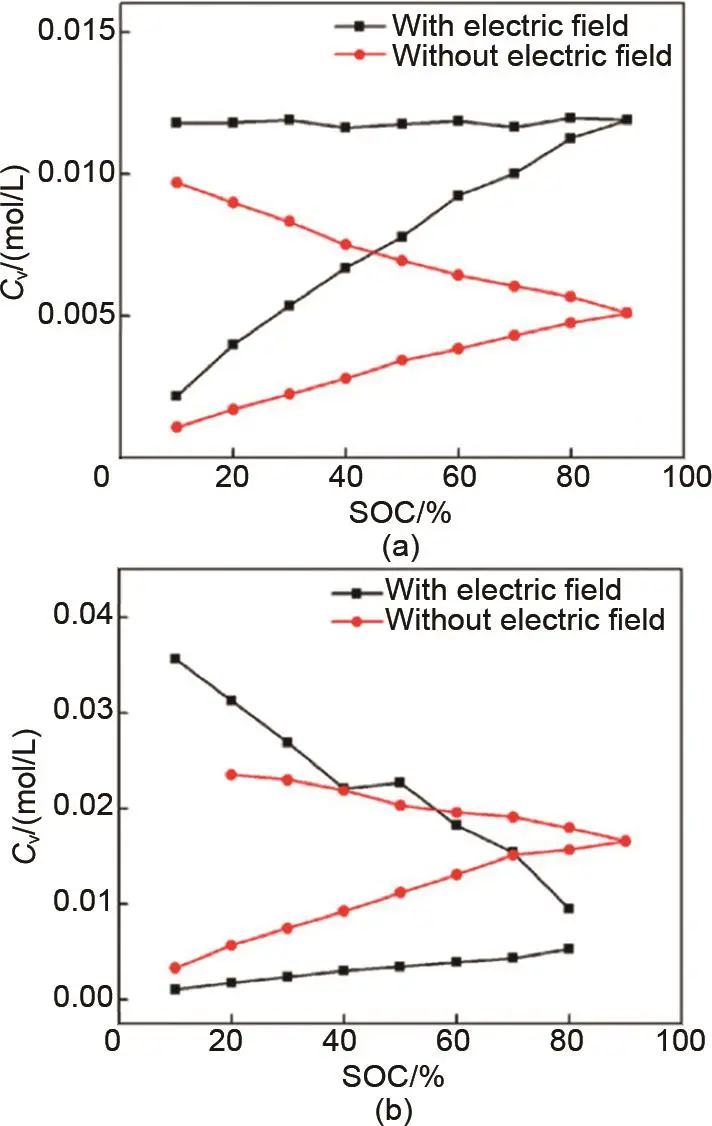
图8 有无电场作用下钒离子的输运行为:(a) 各SOC下,钒离子从VO2+/VO2+侧迁移到Fe3+/Fe2+侧;(b) 各SOC下,钒离子从V3+/V2+侧扩散到Fe2+/Fe3+侧
Cecchetti等人根据三种不同电流密度(10 mA/cm2、40 mA/cm2、100 mA/cm2)下的测试结果,对全钒液流电池运行的一维物理模型进行了校准,得出结论:①较高的工作电流密度增加了充放电循环的速度,可以减少电池自放电和钒交叉引起的电解液不平衡;②在低电流密度下,各价态钒离子的扩散在交叉通量中占比均高于90%,是钒通过膜的主要机制,而在高电流密度下,扩散和电迁移对钒通量的贡献几乎相等(图9)。
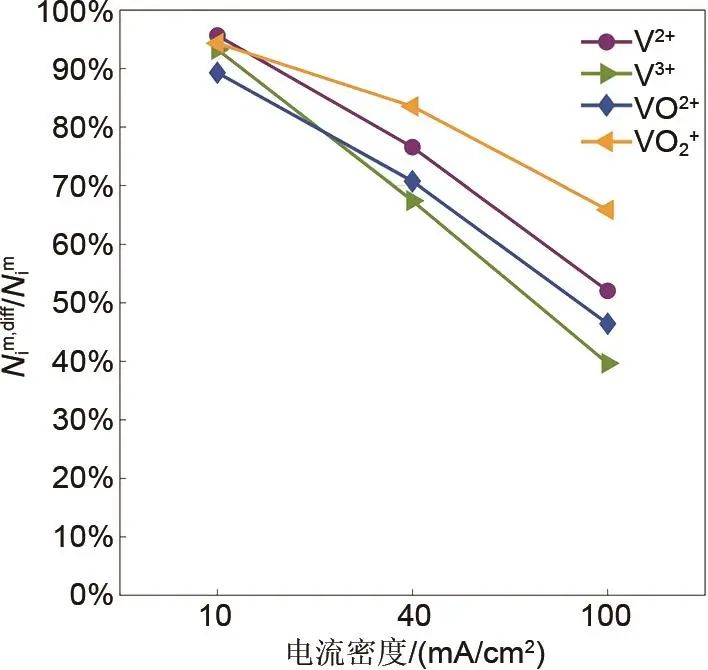
图9 扩散通量对钒离子整体交叉通量的贡献
除了影响钒离子的跨膜渗透,电流密度还影响着电池的充放电行为。在相同截止条件下,随着电流密度的增大,电池极化加剧,充电电压增大,放电电压减小,充放电周期时间减小,钒电池的起始容量随着电流密度的增加而下降。
也就是说,电流密度对电池容量的作用是双向的,高的电流密度会降低电池的起始容量并且导致更快的离子扩散速度,但同时又加快了充放电时间从而减少了离子扩散的时间。因此,采用适当的充放电策略对于钒电池容量衰减抑制是有必要的。
1.2.4 活性物质浓度
在全钒液流电池中,电能以化学能的形式存储于电解液中。提高活性物质的浓度,可以直接提高电池的能量密度与放电容量,但是活性物质浓度较高时,电解液稳定性下降易产生沉淀,反而降低电池容量。此外,电解液中钒离子总是由负极储液罐跨膜渗透至正极储液罐,因此通常采用提升负极渗透压的方式来促进水分子向负极扩散,从而减小钒离子的迁移以抑制容量衰减问题。李君涛等[34]设置了不对称浓度实验(表2),在充放电循环中,降低负极电解液的钒离子浓度并提高其硫酸含量,增加负极液渗透压,减少钒离子和水分子的跨膜扩散,最终减少了电池容量的损失,对称实验、不对称Ⅰ和不对称Ⅱ的容量衰减率分别为0.8、0.66、0.52。
表2 三组正极钒离子浓度测试结果
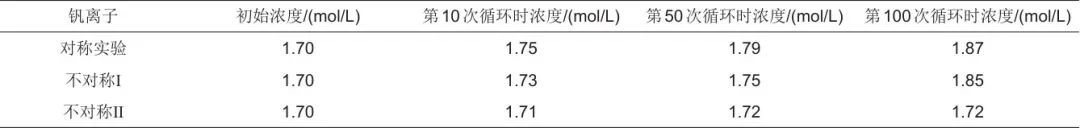
不对称浓度抑制了钒离子和水分子的迁移,对于容量的长久保持是有利的。然而活性物质浓度的不对称导致了正负极电解液未能全部反应,降低了钒离子的利用率,实际上减少了钒电池的总容量。
2 衰减抑制研究
从技术上讲,全钒液流电池的性能不仅取决于电池组件、电荷传输和电催化材料的物理特性,还取决于电池内部复杂流动和物质传输过程的管理。为了抑制全钒液流电池的容量衰减,研究人员将重点放在提高电解液性能以提高钒离子的溶解度和稳定性,提高电极性能以提高电化学可逆性和电化学活性,设计新型膜以降低全钒液流电池中钒离子的交叉和水跨膜传递,同时降低电阻。此外,对于给定的电池组件材料,电池性能的提高还依赖于优化电池结构和运行策略。
2.1 材料改性抑制容量衰减
2.1.1 电解液
通过电解液改性来提高容量及抑制衰减有两种途径:一种是在电解液中添加有益的基团,如在电解液中引入氨基、磺基、羟基、羧基等亲水性官能团。这些添加剂的加入为电极反应提供了更多的活性位点,从而提高了电池容量,并且添加剂可以与钒离子络合,从而提高了电解液的溶解度和稳定性。Hou等人研究了聚丙烯酸(PAA)对V(V)正电解液热稳定性和电化学性能的影响,结果表明:PAA添加剂能提高V(V)的热稳定性,使用含3% PAA的正极电解液溶液的电池在50℃下具有良好的循环性能,其在循环过程中的容量保持率相较于不含PAA的电池提高了约23.76%。
另一种途径是在电解液中加入一种可溶的溶质,以此来提升负极电解液的渗透压,这种方法可使两个半电池中电解液的渗透压差减小,显著降低钒离子的交叉现象。Yan等人受正向渗透(FO)机制(图10)的启发,通过在负极电解液中加入可溶的抽吸溶质(2-甲基咪唑)来抵消正、负半电池之间的渗透压,成功抑制了全钒液流电池容量的下降,结果如图11所示。Chen等人选择糖类添加剂如葡萄糖、蔗糖、D(+)-木糖和α-乳糖一水作为全钒液流电池负极电解液的添加剂,通过引入的羟基增加了V2+/V3+氧化还原反应的活性位点,增强了电极的亲水性,同时为负极电解液增加了额外的渗透压,降低了钒离子交叉,循环30次后容量保留率为71%,比对照组的29.5%提高了41.5%。
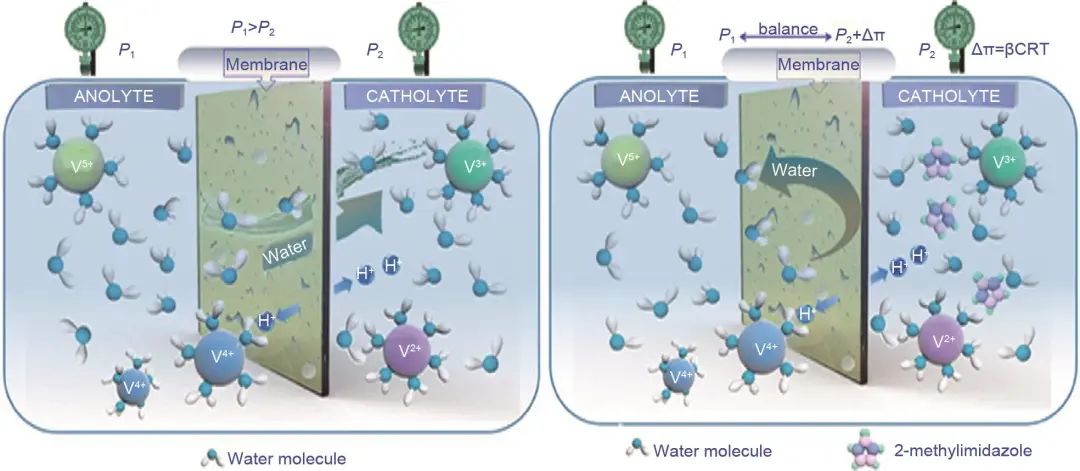
图10 在充放电过程中,抽吸溶质平衡渗透压的示意图
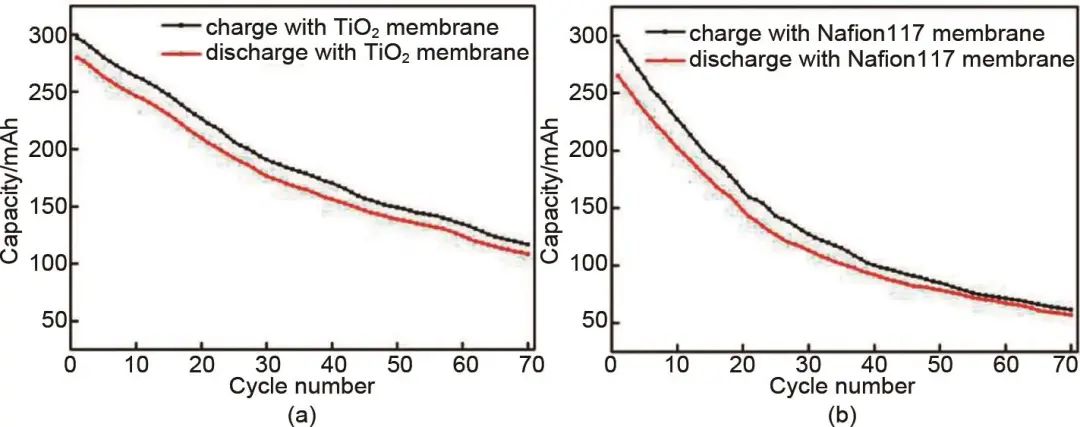
图11 添加2-甲基咪唑对含 (a) TiO2和 (b) Nafion117膜VRFB容量衰减的影响
为应对容量衰减问题,对电解液本身的改性手段主要为使用各种类的添加剂,但无论是有机添加剂或是无机添加剂均有其局限性。大多数有机添加剂具有较高的黏度,导致溶液的电导率降低,电化学传质减弱,因此在选择有机添加剂的同时需控制好黏度参数,这对改善溶液流动性和增强电化学传质具有重要意义。同时,在具有强酸性和氧化性的负极电解液中有机添加剂的长期稳定性较差,在电解液的长期使用中会出现降解、析出等问题,导致电池的性能和寿命下降。无机添加剂在电解液中相当于杂质,通常用来提升电解液的稳定性,但其会导致电解液电化学性能的恶化,因此无机添加剂的引入量不宜过多。此外,添加剂的引入额外增加了电解液制备的成本。
2.1.2 隔膜
物种在膜上的交叉渗透主要有三种运输机制,即:对流、扩散和迁移。物种跨膜运输的速率主要由膜的化学成分决定。为了尽量减少钒离子交叉造成的容量损失,研究人员对隔膜的改性做了大量的工作。
根据膜上基团的不同,隔膜主要有阳离子交换膜、阴离子交换膜、两性离子交换膜、非离子多孔膜等,阳离子交换膜的作用原理如图12所示。目前全钒液流电池中普遍使用的是杜邦公司生产的Nafion系列膜,该膜为阳离子交换膜,其本身具有优秀的离子导电性与氧化稳定性,但同时也存在着离子选择性不足,钒渗透率高的问题。因此,通常通过引入抗钒离子层或与无机材料杂化来降低其钒离子透过率。Ye等人采用溶液混合和浇铸法制备了Nafion/木质素复合膜,通过木质素扩大质子传导通道来促进质子的传输,并降低钒离子的渗透率,从而提高了钒离子的选择性。如图13所示,在120 mA/cm2时,与目前商业化应用的Nafion 212膜相比,使用该复合膜的全钒液流电池在原有效率不变的情况下提升了容量保持率,在150次循环时仍保有48.4%。
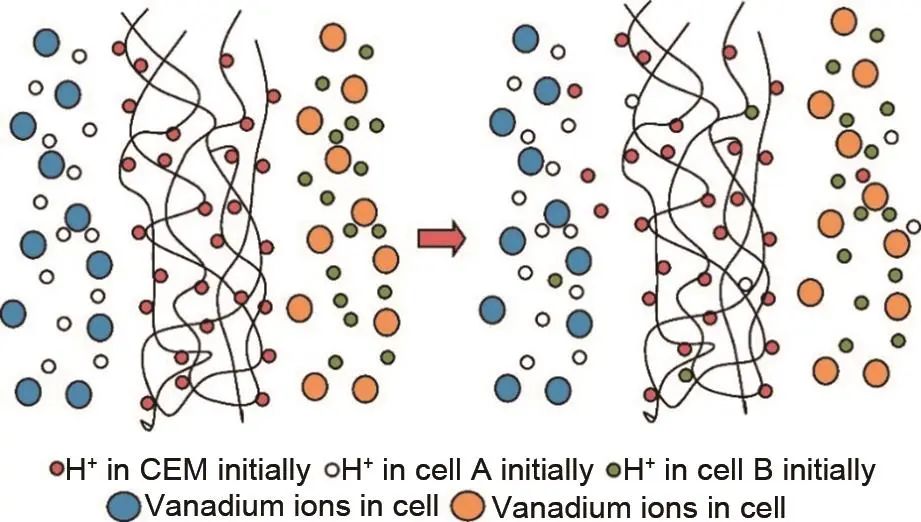
图12 阳离子交换膜的离子交换过程示意图
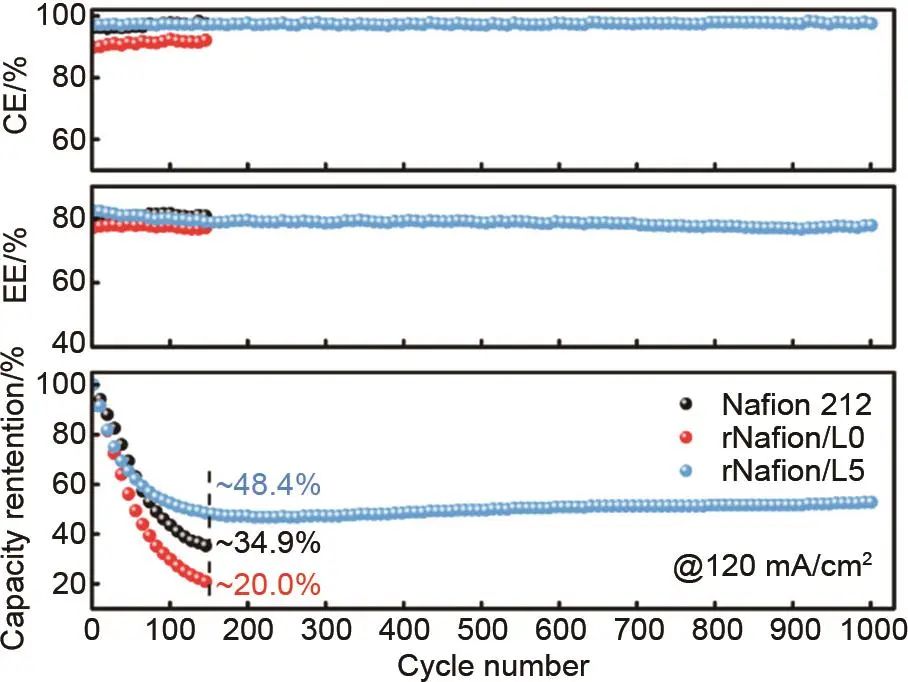
图13 在120 mA/cm2条件下,单层膜电池的效率和放电容量保持情况
阴离子交换膜的使用并不多见,理论上,阴离子交换膜具有较高的阻钒性能,但在电解液中较差的化学稳定性阻碍了其应用。两性离子交换膜同时具有阳离子交换膜和阴离子交换膜的优点,可以提供更高的离子选择和传导能力,但需要控制两种官能团的密度平衡,这导致了制备成本升高,因此大多数的两性离子交换膜研究方向都集中于降低制备成本。多孔膜通过孔径筛分机制来进行离子选择,其成本较低,化学稳定性高,但由于缺少官能团,对于两侧电解液的阻隔作用不强,对于多孔膜的研究广泛集中于缩小孔径或者添加官能团,如能在多孔膜中引入合适的官能团提升其离子选择性,有望在商业化中取代目前的Nafion系列膜。
除了离子的选择透过性,隔膜对于电解液容量的影响还表现在内阻、膜厚等方面。较厚的膜可以减少钒离子的跨膜交叉,但其具有较高的电阻,会增大电池的极化,降低其放电容量;而薄膜虽然降低了内阻,但可能导致更多的钒离子交叉渗透,增加了电解液的不平衡,促进容量衰减。
理想的膜应具有良好的离子交换能力,离子电导率高,吸水率低,膨胀比小,化学稳定性好,以及成本低等特点。而目前钒电池的隔膜无法满足上述所有性能,仍需进一步研究开发,比较有前景的方向主要有以下几个。一是以廉价材料对Nafion膜进行复合制备以降低其成本并提升其阻钒性能;二是采用阻钒率较高的低成本膜如基于SPEEK或SPI的改性阳离子膜,但需继续增加其稳定性与电导率;三是在多孔膜中引入适当的基团增强其离子选择性。值得注意的是,除了隔膜本身物化性能的优化外,膜厚对钒电池性能影响也是需要研究的重点。
2.2 工况控制缓解容量衰减
全钒液流电池中主要的传递问题是钒离子跨膜,不同钒离子在膜内的不平衡输运特性导致了电池循环过程中电解液的不平衡。基于对钒离子跨膜机理的了解,研究者提出了各种工况优化策略来缓解钒离子交叉并抑制相关的电池容量衰减。
2.2.1 电解液流量优化
在关键运行参数中,流量是对液流电池性能影响较大同时也较为复杂的因素。因此,研究人员对其影响和调控策略进行了广泛的研究。Ma等研制了一种千瓦级全钒液流电池系统,研究了电解液流量的各种策略对电池充放电行为和性能的影响,提出了全钒液流电池系统的流量提升策略。该策略在整个主要运行状态下保持恒定的流量,并在充电或放电过程结束时提高流量。具体为在充电过程中,以0.2 m3/h的较低流量运行,然后在电压增加到23.1 V时将流量增加到0.71 m3/h。在放电过程中,同样以0.2 m3/h的较低流量运行,然后在电压降至16.8 V时将流量增加到0.71 m3/h。与始终在0.71 m3/h的高流量下运行相比,系统效率可以提高8%。Tang等人通过模拟浓度过电位并分析所有组件的压力损失,在预设电压截止限制下,确定了形成5 kW/15 kWh全钒液流电池系统的最佳可变流量,证明了连续变流量策略优于定流量策略。Karrech等人通过实验研究化学计量数λ(实际流量/理论流量)为3~18的恒定流量的影响,当λ=3时,电池的容量达到2.093 Ah。将λ增加到6和9,每次增加充电容量可提高5%。将λ增加到12、15和18后,改善率较低为2.81%、1.81%和1.57%。即增加流量可以增加电池的充电容量,但存在一个接近λ=9的饱和点,超过之后改善往往较小。此外,研究发现在充/放电过程时逐渐改变流量策略或突然提高流量策略均可以减少浓度过电位,且两者最终容量接近。
除了影响浓度过电位,流量还影响着钒离子的跨膜扩散通量,Song等人[45]根据达西定律分析了膜上的压降,系统地发展了电解液的传递机理,并通过充放电实验进一步验证。实验结果揭示了两种半电池电解液之间的黏度差对电解液交叉和可用容量衰减的贡献,同时表明高流量可能加快电解液转移的速度。除此之外,实验结果还证明,在测量两种半电池电解液黏度的基础上,通过适当的流量优化,可以有效地抑制电解液的转移,从而实现提高全钒液流电池系统长期充放电循环中的放电容量(图14)。
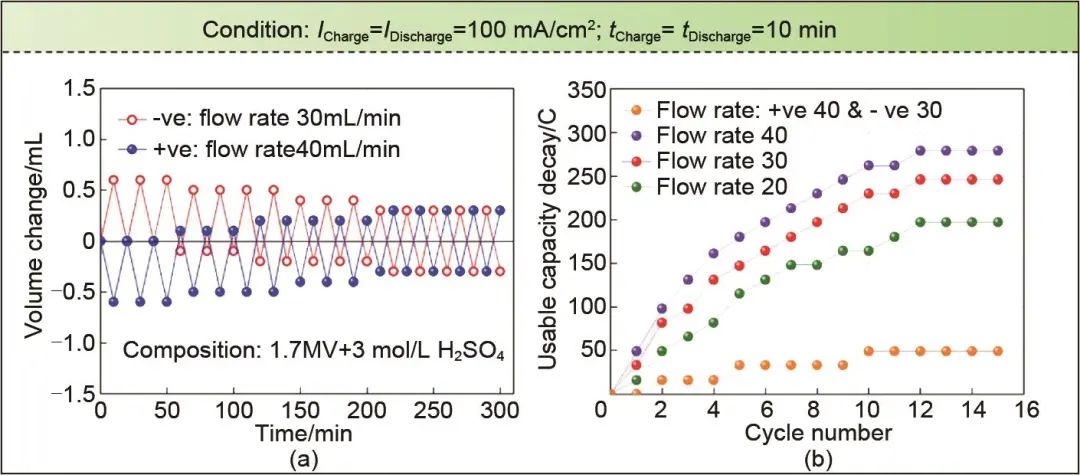
图14 流量优化下的体积变化和容量衰减
充放电末期流量的增加可以为半电池提供更多的反应物,促进氧化还原反应,降低浓度过电位,增大系统容量。然而,只针对浓差极化的流量调节往往忽略了变流量对于钒离子迁移的影响,对于长期循环后的容量保持是不利的。对于衰减抑制方面来说,在降低浓差极化的同时还应结合流量对钒离子迁移的影响,使电池获得最大容量的同时降低其容量衰减率。
2.2.2 充放电制度优化
电流密度是影响全钒液流电池充放电行为和性能的重要参数。一方面,电流密度影响着钒离子的扩散行为;另一方面,工作电流影响着电池的充放电深度、电压极化等方面。Agar等的研究表明,采用不对称电流操作策略(即在保持放电电流恒定的同时增加充电电流)可以抑制容量衰减,其中对流主导膜衰减率降低7.1%,扩散主导膜容量衰减率降低12.4%。该策略提高了充电过程中电渗透对流的强度,通过电渗透对流补偿渗透过程造成的对流交叉,减少了钒离子在膜上的迁移量。Yang等人采用二维准稳态模型,探究了与荷电状态相关的工作电流策略,通过充放电过程结束时低电流,剩余时间采用高电流的方法,提高了系统效率、功率密度和循环内的净放电能量。
充放电截止电压也是容量衰减的影响因素之一,其直接影响析气副反应,Huang等人采用不同的截止电压对全钒液流电池进行充放电循环,评估了截止电压与析氢和氧化反应有关的影响(图15)。研究结果表明,将充电截止参考电压设置为1.65 V时,60次循环后电池容量可保持在61.76%。当充电截止电压每增加0.1 V和0.15 V,电池容量分别减少1.74%和5.16%。
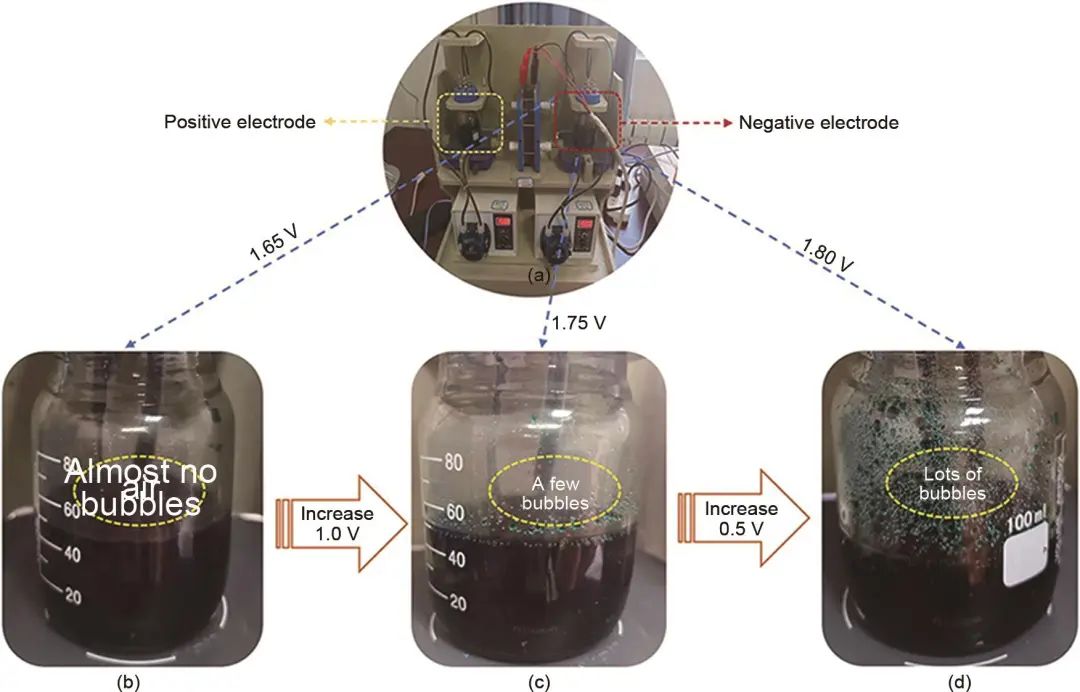
图15 截止电压对析气反应的影响 (a) 单体电池;(b) 1.65 V;(c) 1.75 V;(d) 1.80 V
充放电制度优化包括截止电压与电流密度两个部分,截止电压通常被控制在1~1.55 V以减少电池副反应,电流密度的优化则可以有效控制钒离子的迁移减少容量衰减。目前全钒液流电池较多应用于储能领域,根据调峰、调频的不同需求,全钒液流电池的充放电工况也不相同,根据具体工况采用与荷电状态相关的电流策略有着其必要性。
2.2.3 活性物质浓度优化
与电解液改性类似,活性物质浓度优化也通过调节正、负极渗透压来达到抑制钒离子交叉扩散的目的。不同的是,在电解液改性中,加入其他溶质等同于引入杂质离子,使电解液纯度降低,有些离子还对电化学性能影响较大,而浓度优化通常采用调节钒离子浓度或H2SO4浓度的方式来改变渗透压差,可以在保证全钒液流电池电化学性能的前提下抑制容量衰减,但可能会影响到电池的初始容量及钒离子利用率。Lu等人通过二维等温瞬态模型,研究了不对称电解液浓度(即降低负电解液的初始浓度,同时增加正电解液的初始浓度)对全钒液流电池循环过程中容量衰减行为和钒离子交叉机理的影响。研究发现,在保持负极不变的情况下,增大正极电解液中钒离子的初始浓度,可以有效抑制放电容量的衰减。对称组经46次循环后容量衰减20.5%,而正极钒离子浓度为1.3 mol/L时容量衰减率为13.2%,当其浓度升到2.0 mol/L时,容量基本维持不变,这是由于增大了VO2+、VO2+向负极的扩散通量,减小了电解液浓度失衡的倾向(图16)。
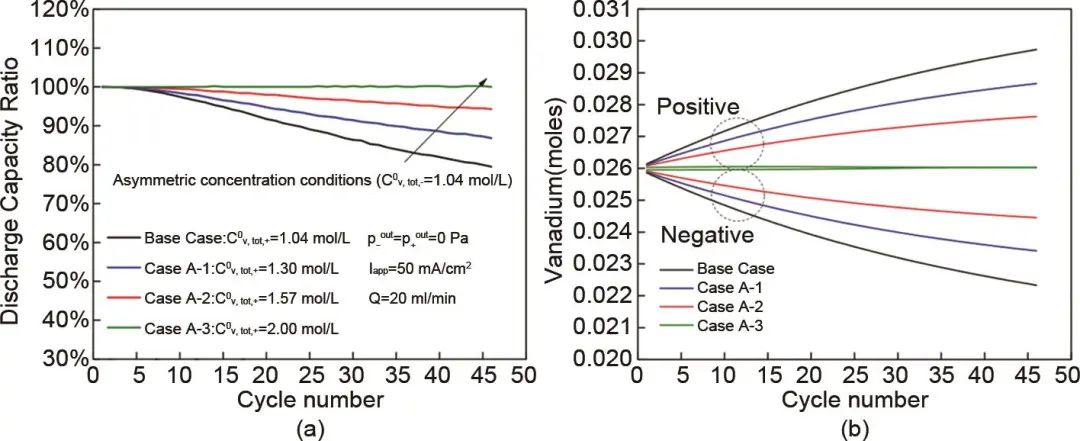
图16 在46次循环中:(a) 不对称浓度策略对放电容量的影响;(b) 不对称浓度策略中钒离子量的变化
此外,当使用添加剂调节电解液渗透压时通常是对负极电解液进行增渗使其吸水性更强,而活性物质的优化是增加正极电解液浓度,这是由于两者渗透压调节机制不同,但本质上都是减小负极电解液向正极迁移的趋势。
3 结 论
全钒液流电池的容量衰减问题主要是由钒离子的跨膜渗透及其后续的副反应等因素造成。基于此种机理,目前最常见的是通过材料改性或者工况优化的方法来抑制其容量衰减。对于材料改性方面,通常对电解液及隔膜进行改性处理,以解决钒离子的迁移问题。对于工况优化方面,由于工况对于容量衰减的影响通常是多方面的,需要考虑多种衰减因素的耦合作用,根据不同工况制定合适的运行策略,但本质上也是降低钒离子跨膜扩散的程度。未来全钒液流电池需要进一步解决的问题包括:
(1)继续深化对容量衰减机理的认知,目前对于钒离子的跨膜行为研究较多,但由于模型和选用参数的差异,研究人员对跨膜的实际机理未有明确的共识。扩散、迁移及对流对于钒离子的贡献未被量化,容量衰减因素需要进一步分析权重,才能正确指导容量衰减抑制方法。
(2)材料改性与工况优化均能对全钒液流电池的容量衰减抑制起到关键作用。先进材料如电解液、隔膜的研发确保了电池的技术革新与突破,未来需要集中于以下方面:对于电解液来说,目前所用添加剂的方法有其局限性,需要开发新体系的电解液如水性和非水性钒体系,以提高电解液密度,增强电解液的稳定性。目前HCl/H2SO4混合支撑电解液开发相对成熟,说明新体系的开发是比较有前景的研究方向。在隔膜方面,需要研发具有更高阻钒率、更低接触电阻以及稳定性更强的改性隔膜,目前较有前景的方向主要有:选用廉价材料对Nafion膜进行复合制备以降低成本并提升其阻钒性能;采用阻钒率较高的低成本膜如基于SPEEK或SPI的改性阳离子膜,但需继续保持稳定性与电导率;在多孔膜中引入适当的基团增强其离子选择性。
在材料选型后,对于工况的优化也是值得关注的方面,对容量衰减抑制较为有效的是流量优化与充放电制度优化,而浓度优化降低了钒离子的利用率因此不宜采用。需要注意的是流量优化应在减小浓差极化的同时关注钒离子的迁移问题,使电池具有高容量的同时维持高容量保持率。充放电制度则应结合实际使用需求,结合荷电状态对其进行优化。





